液态活检
一、 核心定义
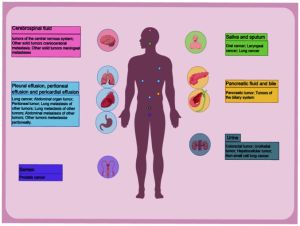
液态活检(又称液体活检)是无创 / 微创获取血液、 脑脊液、 唾液、 胸水、 尿液等体液, 检测其中来自肿瘤或病变组织的循环标志物, 替代传统穿刺 / 手术活检, 实现肿瘤早筛、 诊断、 用药指导、 疗效监测、 复发预警的技术, 是精准医疗的核心工具。
二、 核心标志物(四大类)
1. ctDNA(循环肿瘤 DNA)
- 肿瘤细胞凋亡 / 坏死释放到血液的游离 DNA 片段, 携带肿瘤特有突变、 甲基化、 拷贝数变异。
- 特点: 半衰期短(≈2 小时)、 灵敏度高、 可定量, 是早筛与微小残留病(MRD)监测首选。
2. CTC(循环肿瘤细胞)
- 从原发灶 / 转移灶脱落进入血液的完整肿瘤细胞, 可提示转移潜能与预后。
- 特点: 数量极少(10⁶–10⁷个白细胞中仅 1 个), 富集难度大, FDA 已批准用于乳腺癌、 结直肠癌、 前列腺癌预后。
3. 外泌体(Extracellular Vesicles, EVs)
- 肿瘤细胞分泌的纳米级囊泡(30–150 nm), 携带蛋白质、 mRNA、 miRNA、 脂质、 DNA。
- 特点: 稳定性极强、 含量高、 携带信息全面, 适合早期筛查与转移预测。
4. 其他标志物
- cfRNA: 游离 RNA(mRNA/lncRNA/miRNA), 反映基因表达动态。
- 肿瘤血小板(TEPs): 吸附肿瘤 RNA / 蛋白的血小板, 高特异性。
- 甲基化标志物: ctDNA 甲基化(如SEPT9、 SHOX2), 癌症早期稳定表观标记。
三、 技术原理(怎么测)
样本采集
外周血 5–10 mL(无创, 无需空腹)。分离富集
- ctDNA: 血浆提取游离 DNA → **NGS / 数字 PCR(ddPCR)** 检测突变 / 甲基化。
- CTC: 免疫磁珠 / 微流控芯片特异性捕获 → 染色 / 测序分析。
- 外泌体: 超速离心 / 试剂盒提取 → 蛋白质谱 / RNA 测序。
生物信息分析
比对正常基因组, 识别肿瘤特有变异, 计算突变丰度、 拷贝数、 甲基化水平。结果解读
生成肿瘤风险评分、 用药靶点、 复发风险分层报告。
四、 vs 传统组织活检(关键优势)
| 维度 | 传统组织活检 | 液态活检 |
|---|---|---|
| 创伤性 | 有创(穿刺 / 手术),出血 / 感染风险 | 无创,仅抽血,安全可重复 |
| 取样局限 | 单点取样,异质性漏诊 | 捕获全身肿瘤信号,无偏倚 |
| 时间周期 | 5–7 天出病理 | 1–3 天出分子报告 |
| 适用场景 | 仅能测已发现实体瘤 | 早筛、无法穿刺晚期、复发监测 |
| 动态监测 | 不可重复,滞后 | 实时、连续监测,提前 4–6 个月预警复发 |
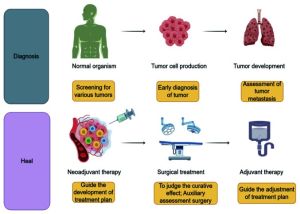
五、 临床应用(全周期覆盖)
1. 早期筛查(最热门)
- 高危人群(吸烟、 家族史、 慢性病史)多癌种早筛(肺癌、 肝癌、 结直肠癌、 胃癌、 胰腺癌、 卵巢癌)。
- 甲基化检测灵敏度≈93%, 早于影像学1–2 年发现肿瘤。
2. 诊断与分型
- 无法穿刺 / 手术的晚期患者, 快速获取基因突变(如 EGFR、 ALK、 KRAS), 指导靶向 / 免疫用药。
- 鉴别原发灶不明转移癌, 提示肿瘤来源。
3. 疗效监测
- 治疗中动态追踪 ctDNA 突变丰度: 下降 = 有效, 上升 = 耐药 / 进展。
- 替代影像学, 提前 4–6 个月发现复发, 及时干预。
4. 微小残留病(MRD)
- 术后ctDNA 阴性 = 低复发风险(5 年生存率 > 90%); 阳性 = 高风险, 需辅助治疗。
5. 预后评估
- CTC 数量越多、 ctDNA 丰度越高, 预后越差、 生存期越短。
六、 核心技术平台
- NGS(二代测序): 金标准, 可测全外显子 / 全基因组, 多突变并行, 适合早筛与用药指导。
- ddPCR(数字 PCR): 超高灵敏度, 可测0.01% 低频突变, 适合MRD 监测。
- 甲基化芯片: 低成本、 高通量, 适合大规模早筛。
- 微流控芯片: CTC 高效富集, 自动化操作。
七、 挑战与局限
灵敏度瓶颈
极早期(I 期)ctDNA 浓度极低, 假阴性率≈20%。假阳性
正常细胞 cfDNA 干扰、 克隆性造血突变, 需严格质控。标准化不足
样本处理、 测序流程、 报告解读缺乏统一标准。成本较高
NGS 全外显子 **≈5000–10000 元 / 次 **, 限制普及。不能替代组织病理
确诊仍需组织活检, 液态活检为补充 / 替代。
八、 总结
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。