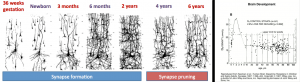
突触修剪
突触修剪(synapse pruning),包括轴突和树突完全衰退和死亡,是在许多哺乳动物(包括人类)的幼年期和青春期开始之间发生的突触消除过程。到成年时,婴儿大脑的大小将增加多达5倍,最终达到约86(±8)亿个神经元的大小。有两个因素促成了这种增长:神经元之间的突触连接的增长,以及神经纤维的髓鞘化。然而,神经元的总数保持不变。修剪受环境因素的影响,被广泛认为代表学习的机制之一。青春期后,由于突触修剪,突触连接的体积再次减少。
调节性修剪编辑本段
出生时,视觉和运动皮层的神经元与上丘、脊髓和脑桥相连。每个皮层的神经元都被选择性地修剪,留下与功能上适当的处理中心的连接。因此,视皮层的神经元切断与脊髓神经元的突触,运动皮层切断与上丘的连接。这种变化的修剪被称为大规模定型轴突修剪。神经元将长轴突分支发送到适当和不适当的靶区,不适当的连接最终被剪除。
回归事件改善了神经发生中的大量连接,从而形成一个特定的成熟电路。细胞凋亡和剪枝是切断不想要的连接的两种主要方法。在细胞凋亡中,神经元被杀死,与神经元相关的所有连接也被消除。相反,神经元在修剪时不会死亡,但需要轴突从功能上不合适的突触连接处缩回。
人们认为,突触修剪的目的是从大脑中移除不必要的神经元结构;随着人类大脑的发展,理解更复杂结构的需要变得更具针对性,儿童时期形成的更简单的联系被复杂结构所取代。
尽管它与儿童认知发育的调节有着许多关联,但修剪被认为是一个去除神经元的过程,神经元可能已经受损或退化,以进一步提高大脑特定区域的“网络”能力。在发育和修复方面起作用,但同时也是通过突触效率去除神经元来持续维持更有效的大脑功能的一种手段。
在成熟的大脑中修剪编辑本段
与学习相关的修剪被称为小规模轴突末端修剪。轴突向目标区域内的神经元延伸短轴突末端。某些终端被竞争修剪。修剪后的终端的选择遵循突触可塑性中的“使用或丢失”原则。这意味着经常使用的突触具有很强的连接,而很少使用的突触则被排除。在脊椎动物身上看到的例子包括修剪周围神经系统神经肌肉连接处的轴突末端和修剪中枢神经系统小脑的攀缘纤维输入。
就人类而言,通过推断儿童和成人之间神经胶质细胞和神经元的估计数量的差异,观察到了突触修剪,这在中嗅丘脑核中有很大差异。
在牛津大学2007年进行的一项研究中,研究人员根据体视分级收集到的大小和证据,将8个新生大脑与8个成年人的大脑进行了比较。他们发现,在他们测量的中餐丘脑核区域,成人神经元数量的平均估计值比新生儿低41%。
然而,就神经胶质细胞而言,成人的估计要比新生儿大得多;成人的平均脑容量为3630万,而新生儿的平均脑容量为1060万。在一些研究中,在发育的情况下,通过程序性细胞死亡而失去的神经元不太可能被再利用,而是被新的神经元结构或突触结构所取代,并且被发现与皮质下灰质的结构变化同时发生。
突触修剪与老年时的突触退化事件要分开。尽管发育性修剪依赖于经验,但与老年突触的消失却不同。
机制编辑本段
解释突触修剪的三个模型是轴突退化、轴突收缩和轴突脱落。在所有情况下,突触都是由一个短暂的轴突末端形成的,而突触的消除是由轴突的修剪引起的。每种模型都提供了一种不同的方法,即去除轴突来删除突触。在小规模轴突修剪中,神经活性被认为是一个重要的调节机制,但其分子机制尚不清楚。激素和营养因子被认为是调节大规模定型轴突修剪的主要外在因素。
轴突变性
果蝇的神经系统在变态过程中发生了广泛的变化。蜕变是由蜕皮酮引发的,在这一时期,神经网络发生了广泛的修剪和重组。因此,理论上果蝇的修剪是由蜕皮酮受体的激活触发的。脊椎动物神经肌肉连接处的去神经研究表明,轴突去除机制与Wallerian变性非常相似。然而,果蝇的整体和同时修剪与哺乳动物神经系统修剪不同,后者发生在局部和多个发育阶段。
轴突收缩
轴突分支以远端到近端的方式收缩。收缩的轴突内容物被认为被循环到轴突的其他部分。哺乳动物中枢神经系统轴突修剪的生物学机制尚不清楚。然而,修剪与小鼠体内的引导分子有关。引导分子通过排斥作用控制轴突的寻路,并开始修剪大量的突触连接。信号素配体和受体神经纤毛和神经丛素被用来诱导轴突的收缩,从而启动海马间隔和锥体下束(IPB)的修剪。在有Plexin-A3缺陷的小鼠中,海马投射的刻板修剪被发现明显受损。具体来说,一旦Plexin-A3受体被3类信号素配体激活,与瞬时靶点相连的轴突将收缩。在IPB中,SEMA3F的mRNA表达存在于出生前的海马体、出生后丢失的海马体和返回的地层中。巧合的是,开始的IPB修剪发生在同一时间。在海马间隔投射的情况下,3天后开始修剪,然后表达SEMA3A的mRNA。这表明,一旦配体在检测到的mRNA表达后的几天内达到阈值蛋白水平,就会触发剪枝。神经纤毛蛋白-2突变体和Plexin-A3和Plexin-A4双突变体小鼠的视皮质脊髓束(CST)轴突的剪枝是有缺陷的。在修剪过程中,SEMA3F也在脊髓背侧表达。在这些突变体中没有观察到电机CST修剪缺陷。
也观察到从视网膜顶部形成过度延伸轴突分支裁剪。已发现,肾上腺素和肾上腺素受体(EPH)可调节和引导视网膜轴突分支。在肾素A和EPHA之间,沿着前后轴的正向信号传导被发现可以抑制终末区后的视网膜轴突分支的形成。正向信号也促进了到达末端区域的轴突的修剪。然而,目前还不清楚IPB修剪中的收缩机制是否应用于视网膜轴突。
已发现,在eph受体酪氨酸激酶和eph-b蛋白之间存在反向信号传导,从而启动了ipb的收缩机制。在海马轴突中观察到,eprin-b3可将酪氨酸磷酸化依赖的反向信号转导,从而触发过度IPB纤维的剪枝。所提出的途径包括在靶细胞表面表达ephb,从而导致ephrin-b3的酪氨酸磷酸化。随后,ephrin-b3与细胞质衔接蛋白grb4结合,导致dock180和p21激活激酶(pak)的募集和结合。dock180的结合增加了rac gtp水平,pak介导了主动rac的下游信号,从而导致轴突的收缩并最终修剪。
轴突脱落
小鼠神经肌肉连接处轴突后退的延时成像显示轴突脱落是一种可能的修剪机制。后退的轴突从远端向近端移动,类似于回缩。然而,在许多病例中,当轴突收缩时,残余物脱落。这些被称为轴突体的残余物,包含着与轴突末端相连的鳞茎中相同的细胞器,通常在鳞茎附近发现。这表明轴突源于鳞茎。此外,轴突没有电子密集的细胞质或破坏的线粒体,这表明轴突不是通过Wallerian变性形成的。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。