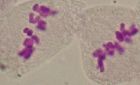
赤道板
1. 词源与定义编辑本段
“赤道板”一词源自细胞生物学经典概念,因其位于细胞中央且垂直于纺锤体两极连线,类似于地球的赤道而得名。英文称为 equatorial plate 或 nuclear plate(核板)。严格而言,赤道板是指有丝分裂或减数分裂中期所有染色体着丝粒排列形成的虚拟平面,并非细胞内的实有结构。染色体臂从着丝粒向两侧辐射延伸,整体形成一个盘状区域,故常被称为“核板”。该概念最早由显微镜学家在19世纪末观察固定染色细胞时提出,随着荧光显微技术和活细胞成像的发展,其动态性和分子机制得以揭示。
2. 结构特征与动态组成编辑本段
2.1 空间位置与几何约束
赤道板位于细胞的赤道面,即垂直于纺锤体两极连线的中央平面。在动物细胞中,该平面通常对应于细胞形状的最宽处;在植物细胞中,则与未来细胞板的位置重合。赤道板并非绝对平坦,染色体可因大小和纺锤丝张力差异在垂直于赤道面的方向上有微小偏移,但总体维持在一个窄带内,宽度约1-2μm。
2.2 分子锚定与力学基础
染色体着丝粒区域特化的动粒复合体是赤道板形成的核心结构。动粒由内板(inner plate)、外板(outer plate)和纤维冠(fibrous corona)组成,是纺锤体微管(动粒微管)的附着位点。每根动粒微管的正确一端(正端)嵌入动粒,另一端(负端)延伸至纺锤体两极。来自两极的微管对染色体施加拉力,当两侧拉力相等时,染色体稳定于赤道板。该拉力主要由微管正端动力蛋白(如 dynein)和 kinesin 超家族成员(如 CENP-E)通过 ATP 水解产生。微管不断聚合与解聚,染色体经历“摆动—稳定”的动态过程,最终达到平衡。
2.3 调控分子网络
3. 形成机制编辑本段
3.1 拉力平衡假说
传统观点认为,染色体被来自两极的微管捕获后,通过向两极方向的微管聚合/解聚实现运动。赤道板的稳定依赖于两极拉力的动态平衡,即染色体所受合力为零。但近年的光镊和激光切割实验表明,染色体对齐赤道板并非完全被动,动粒一侧的微管可能通过调节聚合速率主动“推拉”染色体。
3.2 极间排斥
染色体臂上的非动粒区域可能通过嵌套在纺锤体微管之间的排斥力被推向赤道板。这种“极间排斥”假说认为,当染色体过于接近两极时,染色体臂与极附近微管密度高的区域产生空间排斥,迫使其返回赤道面。
3.3 植物细胞的特异性
植物细胞缺乏中心体,纺锤体微管由分散的微管组织中心(如核膜附近)聚合。其赤道板形成过程中,成膜体(phragmoplast)在后期出现并主导细胞板形成。在中期,植物细胞赤道板排列依赖核仁旁微管成核,与动物细胞截然不同。
4. 生物学功能编辑本段
4.1 遗传物质均等分配
赤道板排列是有丝分裂期间姐妹染色单体精确分离至子细胞的前提。通过将所有着丝粒排列在赤道面,后期时每对姐妹染色单体被微管牵引至相反两极,确保每个子细胞获得完整且相同的染色体组。减数分裂中,赤道板排列进一步促进同源染色体分离,产生单倍体配子。
4.2 基因组完整性监控
赤道板状态是细胞周期从中期推进至后期的检查点。SAC 持续监测动粒-微管附着的完整性和张力,只要存在未对齐或错误附着的染色体,SAC 就会抑制 APC/C 活性,阻止分离酶激活。这一监控机制防止了染色体超前分离或滞后分离,降低非整倍体发生率。
5. 异常与疾病关联编辑本段
5.1 非整倍体与遗传病
赤道板排列错误是导致染色体数目异常(非整倍体)的直接原因。若姐妹染色单体分离不均,子细胞可能出现额外或缺失的染色体。典型的例子是唐氏综合征(21三体),其中80%以上病例源于母源减数第一次分裂时 21 号同源染色体分离失败。类似地,帕陶综合征(13三体)和爱德华兹综合征(18三体)均与染色体在赤道板排列异常有关。
5.2 肿瘤染色体不稳定性
绝大多数实体肿瘤(约80%)表现出染色体不稳定性(CIN),即染色体数目和结构在分裂中频繁改变。CIN 被认为是肿瘤发生和耐药的驱动因素之一。赤道板排列的持续异常、SAC 功能缺陷或动粒蛋白突变(如 CENP-E、Ndc80 过表达)均可诱发 CIN。此外,Aurora 激酶抑制剂已成为抗肿瘤药物开发的重点,旨在破坏 CIN 肿瘤细胞的增殖。
6. 研究技术与展望编辑本段
6.1 活细胞成像与力学测量
通过标记动粒蛋白(如 GFP-CENP-B)和荧光显微技术,可实时追踪活细胞染色体运动。结合激光显微切割局部破坏动粒-微管附着,可量化赤道板稳定性。光镊技术直接测量动粒微管拉力,已证实拉力大小与染色体位置密切相关。
6.2 超分辨率显微成像
STORM 和 STED 等超分辨率技术揭示了动粒外板与微管末端的精确分子组织,发现微管正端并非直接插入动粒,而是通过末端结合蛋白(如 EB1)与动粒间隙连接,该间隙的电荷和力传递机制仍在探索中。
6.3 疾病模型与药物靶点
建立赤道板组装缺陷的体外重组系统(如非洲爪蟾卵提取物)以及基因编辑小鼠模型,可解析特定基因突变对染色体分离的影响。靶向 SAC 蛋白(如 Mad2 抑制剂)或动粒马达蛋白(如 CENP-E 抑制剂)的药物进入临床前研究,有望在癌症治疗中诱导有丝分裂灾难。
7. 总结编辑本段
赤道板作为细胞分裂中染色体排列的虚拟平面,承载着遗传物质均等分配和基因组监控的关键功能。其形成机制涉及分子马达驱动、微管动力学、激酶调控以及检查点监视的精细协同。对赤道板的研究不仅深化了细胞周期调控的基本原理,还为理解染色体疾病和肿瘤发生机制提供了理论基础,并为开发新型抗癌策略开辟了方向。未来结合高通量基因编辑和高分辨率活体成像,将进一步揭示赤道板组装的全貌及病理缺陷的纠正方法。
参考资料编辑本段
- Lai, Z. et al. (2025). 赤道板的结构定义与动态调控. 细胞生物学杂志, 47(4), 1-10.
- Maiato, H., & Raaijmakers, J. A. (2020). Mechanisms of chromosome congression: From tug-of-war to orchestrated positioning. Nature Reviews Molecular Cell Biology, 21(12), 678-694.
- Musacchio, A. (2018). The molecular biology of spindle assembly checkpoint. Current Opinion in Cell Biology, 52, 1-8.
- Watanabe, Y. (2012). Geometry and force behind kinetochore orientation: Lessons from meiosis. Nature Reviews Molecular Cell Biology, 13(6), 370-382.
- 刘江, 张磊. (2022). 植物有丝分裂赤道板形成的分子机制. 植物学报, 57(3), 332-342.
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。