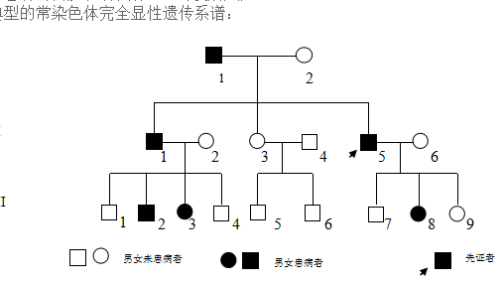
常染色体显性遗传
定义与基本原理编辑本段
常染色体显性遗传(autosomal dominant inheritance)是单基因遗传病中最常见的遗传方式之一,指致病基因位于1-22号常染色体上,且只要一个拷贝的突变等位基因即可导致疾病表型。在杂合子状态下,突变等位基因足以抑制或超越野生型等位基因的功能,从而引发临床异常。该模式遵循孟德尔分离定律,在系谱中呈现典型的垂直传递特征。
遗传学特征编辑本段
常染色体显性遗传疾病的系谱分析显示以下核心特征:第一,疾病连续出现在每一代中,无世代跳跃;第二,患者的父母一方通常为患者,但新发突变可导致散发病例;第三,男女患病概率相等,且患者可将疾病传递给任何性别的后代;第四,患者与正常人婚配时,子代患病风险为50%;第五,完全外显时,患者为杂合子,纯合子往往更为严重甚至致死。外显率与表现度是重要修饰因素,外显率指携带突变基因的个体最终表现出疾病的概率,而表现度指同一突变在不同个体间疾病严重程度的差异。
分子机制编辑本段
常染色体显性遗传病的致病机制主要分为四类:单倍剂量不足(haploinsufficiency):突变导致野生型蛋白产量减半,不足以维持正常生理功能,如弹性蛋白基因突变引起的主动脉瓣上狭窄;显性负效应(dominant negative):突变蛋白干扰野生型蛋白的功能,形成无功能复合物,如COL1A1突变导致的成骨不全症;功能获得突变(gain-of-function):突变蛋白获得异常活性或新功能,如亨廷顿蛋白的多聚谷氨酰胺扩展导致神经毒性;毒性蛋白聚集:错误折叠的突变蛋白在细胞内聚集形成包涵体,损害细胞功能,见于多种神经退行性疾病。
临床常见疾病编辑本段
常染色体显性遗传病涵盖全身各系统,典型代表包括:亨廷顿病(Huntington disease),由HTT基因CAG重复序列扩增引起,特征为进行性运动障碍、认知衰退和精神症状;家族性高胆固醇血症(familial hypercholesterolemia),LDLR基因突变导致低密度脂蛋白受体缺陷,血浆胆固醇显著升高,早发冠心病风险增高;马凡综合征(Marfan syndrome),FBN1基因突变导致原纤蛋白-1缺陷,表现骨骼、眼和心血管系统异常,如主动脉瘤;神经纤维瘤病I型(neurofibromatosis type I),NF1基因突变引起神经纤维瘤、咖啡斑及Lisch结节;多囊肾病(polycystic kidney disease),PKD1或PKD2基因突变导致肾脏多发囊肿及肾功能进行性下降;遗传性乳腺癌(hereditary breast cancer),BRCA1/BRCA2基因突变显著增加乳腺癌和卵巢癌风险。
诊断策略编辑本段
诊断流程包括详细的家系调查与系谱绘制、临床表型评估及分子遗传学检测。基因检测技术从Sanger测序逐步发展为高通量测序(NGS),包括靶向基因panel、全外显子组测序和全基因组测序。对于新发突变或低外显率突变,需结合功能验证实验(如表达分析、酶活性测定)明确致病性。产前诊断和植入前遗传学检测(PGD)可用于高风险的知情生育选择。
治疗与管理编辑本段
目前多数常染色体显性遗传病尚无根治手段,治疗以症状管理、预防并发症和改善生活质量为核心。针对特定分子机制的新型疗法不断涌现:基因沉默:利用反义寡核苷酸或RNAi技术抑制突变等位基因表达,如亨廷顿病中的ASO疗法;酶替代疗法:对溶酶体贮积症等补充缺失的酶;小分子药物:靶向突变蛋白的稳定或功能,如针对转甲状腺素蛋白淀粉样变性的氯苯唑酸;基因编辑:CRISPR-Cas9技术可精准修正突变,但目前仍处于临床前或临床试验阶段。此外,患者应接受遗传咨询,了解疾病遗传风险、生育选择及心理支持。
前沿研究编辑本段
外显率与修饰基因:全基因组关联分析(GWAS)揭示了大量影响疾病表现度的修饰位点,为解释表型异质性提供线索;非编码区突变:在调控区域发现的突变逐渐被证实可通过影响基因表达而致病;体细胞嵌合:部分患者因早期胚胎体细胞突变而呈现较轻或局灶性症状;适应性及进化:某些显性突变可能曾被选择(如疟疾抗性),维持其在人群中的频率。
结语编辑本段
常染色体显性遗传作为最基本的遗传模式之一,其研究与临床实践深刻推动了医学遗传学的发展。从孟德尔时代的经典系谱分析到现代精准医疗,对该类疾病认知的深化不仅提升了诊断准确率,更为靶向治疗开辟了道路。随着基因编辑技术的成熟,根治部分显性遗传病已现曙光,但伦理与安全性问题仍需审慎考量。未来,整合多组学数据、人工智能辅助诊断及个体化治疗策略将进一步改善患者预后。
参考资料编辑本段
- Nussbaum RL, McInnes RR, Willard HF. Thompson & Thompson Genetics in Medicine. 8th ed. Philadelphia: Elsevier; 2016.
- Strachan T, Read AP. Human Molecular Genetics. 5th ed. New York: Garland Science; 2019.
- Korf BR, Irons MB. Human Genetics and Genomics. 4th ed. New York: Wiley-Blackwell; 2013.
- Peach EK, Choi P, Gifford DK. Principles of Clinical Genetics. New York: Springer; 2021.
- Yan H, Dobyns WB, Ruiz-Gómez A, et al. Autosomal dominant inheritance: molecular mechanisms and clinical implications. Annu Rev Genomics Hum Genet. 2020;21:197-220.
- Zhao Y, Zhang Z, Liu J. Advances in gene therapy for autosomal dominant disorders. Nat Rev Genet. 2022;23(5):285-300.
- Lupski JR. Genomic disorders: genome architecture and mutation mechanisms. Cold Spring Harb Perspect Biol. 2017;9(8):a023747.
- Hoffman JD, Grebe TA, Legg SE, et al. Comprehensive genetic testing for autosomal dominant diseases: a clinical update. J Genet Couns. 2023;32(1):1-15.
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。