先导编辑
核心定义与起源编辑本段
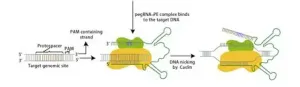
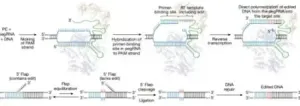
先导编辑(Prime Editing, PE)是 2019 年由哈佛大学 David Liu 团队开发的无 DNA 双链断裂(DSB)、 无需外源供体 DNA的精准基因编辑技术。 它通过Cas9 切口酶(nCas9)- 逆转录酶(RT)融合蛋白与先导编辑向导 RNA(pegRNA)协同工作, 在靶位点仅切开 DNA 单链, 再以 pegRNA 携带的模板直接逆转录写入编辑序列, 实现 “搜索 - 替换” 式精准修改。 该技术可完成全部 12 种碱基转换、 小片段插入(≤44 bp)与缺失(≤80 bp), 大幅降低脱靶与染色体重排风险, 弥补了传统 CRISPR-Cas9 依赖 DSB、 碱基编辑(BE)仅能实现部分碱基转换的局限。 先导编辑的问世, 标志基因编辑进入 “精准涂改” 新时代, 为遗传病根治、 肿瘤治疗、 农业育种等领域提供革命性工具。
三大核心研究方向编辑本段
1. 编辑机制与效率优化
聚焦解析nCas9-RT-pegRNA 三元复合物作用机制, 探究 pegRNA 结构(PBS 与 RTT 长度 / 位置)、 融合蛋白改造、 细胞修复通路对编辑效率的影响。 通过工程化改造 pegRNA(如 epegRNA、 npegRNA)、 优化逆转录酶活性、 筛选高特异性 nCas9 变体, 解决传统 PE 效率低、 稳定性差的问题, 提升精准编辑效率。
2. 疾病精准治疗与模型构建
主攻单基因遗传病、 罕见病、 肿瘤的精准修复, 包括镰状细胞贫血、 血友病、 遗传性酪氨酸血症、 儿童交替性偏瘫(AHC)等。 利用 PE 构建疾病细胞 / 动物模型(如 EGFR 突变肺癌细胞、 ATP1A3 突变小鼠), 用于致病机制研究与药物筛选; 同时探索体内原位编辑策略, 推动从 “对症治疗” 向 “根治” 跨越。
3. 递送系统与安全质控研发
开发适配 PE 的高效、 低免疫原性递送载体, 包括 AAV 病毒载体、 脂质纳米颗粒(LNP)、 核糖核蛋白(RNP)复合物等, 解决体内外递送效率低、 组织靶向性差的瓶颈。 建立脱靶检测技术体系(如 CIRCLE-seq、 rhAmpSeq), 优化编辑后质控流程, 构建安全风险预警模型, 为临床转化提供保障。
关键技术进展编辑本段
1. 核心系统迭代(PE1→PE7)
从初代 PE1(nCas9-MMLV RT 融合蛋白 + pegRNA)迭代至 PE7, 通过 ** 双突变 nCas9(H840A+N863A)** 降低非预期 indel(降低 60%)、 工程化 RT提升逆转录效率、 ** 拆分系统(sPE)** 适配双 AAV 递送, 编辑效率与特异性显著提升。 其中, TwinPE可插入长达 40 kb 的大片段 DNA, 为大片段突变疾病(如亨特综合征)提供解决方案。
2. pegRNA 工程化创新
3. 脱靶规避与靶向范围拓展
4. 体内递送与编辑技术
应用前景编辑本段
1. 遗传病与罕见病精准治疗
可修复约89% 已知致病性人类遗传突变, 包括单基因遗传病(镰状细胞贫血、 β- 地中海贫血)、 罕见病(AHC、 慢性肉芽肿病、 早衰症)。 2025 年 5 月, PE 首次用于人体临床试验, 成功治疗慢性肉芽肿病(CGD)患者, 验证了临床安全性与有效性; 在 AHC 小鼠模型中, 单次脑部注射可实现 85% 突变修正率, 显著改善运动与认知缺陷, 延长生存期。
2. 肿瘤精准治疗与药物研发
3. 农业育种与合成生物学
4. 基础研究与疾病机制解析
生物安全与伦理编辑本段
1. 生物安全风险
2. 伦理规范问题
总结编辑本段
先导编辑作为第三代基因编辑技术, 凭借无 DSB、 高精准、 低脱靶、 编辑类型全面的核心优势, 突破了传统 CRISPR-Cas9 与碱基编辑的技术瓶颈, 实现了基因编辑从 “剪切粘贴” 到 “精准涂改” 的跨越。 目前, PE 技术已完成从机制解析、 工具迭代到临床前验证的关键跨越, 在遗传病治疗、 肿瘤精准干预、 农业育种等领域展现出巨大应用潜力, 2025 年人体临床试验的成功更是标志其正式进入临床转化阶段。
现阶段, 先导编辑仍面临体内递送效率不足、 组织靶向性差、 编辑成本高、 长期安全性数据缺乏等挑战。 未来需重点突破高效靶向递送技术、 优化编辑系统降低成本、 开展长期安全性随访研究、 完善伦理监管体系, 推动先导编辑从实验室走向普惠医疗与农业生产, 为人类健康与粮食安全提供革命性解决方案。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。