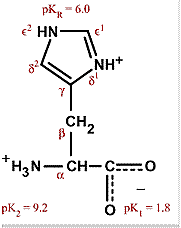
组氨酸
基本信息编辑本段
组氨酸是一种含有咪唑环的α-氨基酸,是蛋白质的组成成分之一。它在生理pH值下,其侧链的咪唑基团具有接近中性的pKa值,这使得它在多种酶的催化中心和蛋白质功能位点中扮演独特的质子供体/受体角色,成为关键的“多功能”氨基酸。 ADSFAEQWER353423413434
| 项目 | 详细信息 |
|---|---|
| 系统命名 | (2S)-2-氨基-3-(1H-咪唑-5-基)丙酸 |
| 英文三字母缩写 | His |
| 英文单字母缩写 | H |
| 化学式 | C₆H₉N₃O₂ |
| 分子量 | 155.15 g/mol |
| CAS号 | 71-00-1(L-型) |
| 分类 | 必需氨基酸(对婴幼儿为条件必需);带正电荷的碱性氨基酸(生理pH下部分质子化) |
| 等电点 | 7.59 |
| 侧链pKa | 咪唑基团 pKa ≈ 6.0 |
| 独特性质 | 侧链咪唑环具有芳香性,在生理pH下可发生互变异构,是高效的亲核试剂 |
化学与结构特性编辑本段
组氨酸的核心特征是其含氮五元咪唑环侧链。
ADFASDFAF23RQ23R
生物合成与代谢编辑本段
生物合成(微生物和植物)
在微生物和植物中,组氨酸的合成途径是一个复杂而古老的保守通路,由10步酶促反应完成,起始于5'-磷酸核糖-1-焦磷酸和ATP。该途径与嘌呤核苷酸代谢有交集,是其前体咪唑甘油磷酸。 ADFASDFAF23RQ23R
人类代谢与需求
生物学功能与意义编辑本段
作为蛋白质的结构与功能元件
- 酶的催化中心:大量水解酶、转移酶、裂合酶的活性中心都含有组氨酸残基,通过其咪唑基团进行广义的酸碱催化(如胰凝乳蛋白酶、磷酸甘油酸变位酶)。
- 金属蛋白的配体:作为金属结合位点,参与电子传递和底物活化(如血红蛋白/肌红蛋白的近端组氨酸固定血红素)。
- 氧传感器:在血红蛋白中,其远端组氨酸通过氢键稳定结合的氧分子,并影响氧亲和力。
- 蛋白质相互作用界面:其芳香性和电荷特性使其常出现在蛋白质-蛋白质、蛋白质-核酸的相互作用界面。
作为关键生物活性分子的前体
这是组氨酸最著名的功能之一。 ADFASDFAF23RQ23R
- 组胺:由组氨酸脱羧生成。是强大的炎症介质、过敏反应的核心物质、胃酸分泌的刺激剂和中枢神经系统中的神经调质。其受体(H₁, H₂, H₃, H₄)是多种重要药物的靶点。
- 肌肽:由组氨酸和β-丙氨酸组成的二肽,大量存在于肌肉和脑组织中,作为pH缓冲剂、抗氧化剂和可能的神经调节剂。
- 鹅肌肽:存在于脊椎动物骨骼肌中的甲基化肌肽类似物。
- 尿刊酸:皮肤中的组氨酸在组氨酸氨裂合酶作用下生成尿刊酸,是表皮天然紫外线吸收剂,并参与免疫调节。
其他生理作用
临床意义与相关疾病编辑本段
组氨酸血症
一种罕见的常染色体隐性遗传代谢病,由组氨酸酶缺乏引起,导致血液和尿液中组氨酸水平升高,尿刊酸减少。大多数患者无症状,但部分可能出现言语发育迟缓和轻度智力障碍,机制可能与组胺或代谢中间物对神经系统的影响有关。
ADSFAEQWER353423413434
组胺相关疾病
组胺代谢或信号异常导致多种疾病: ADSFAEQWER353423413434
- 过敏性疾病:如过敏性鼻炎、哮喘、荨麻疹,由变应原触发肥大细胞释放组胺引起。
- 胃酸相关疾病:组胺是壁细胞分泌胃酸的最强生理刺激物,H₂受体拮抗剂是经典抑酸药。
- 肥大细胞增生症:一组以肥大细胞在组织中异常增殖和聚集为特征的疾病,症状与组胺等介质释放有关。
营养与治疗
- 营养不良/吸收障碍:长期蛋白质-能量营养不良或严重肠道疾病可能导致组氨酸缺乏。
- 类风湿关节炎:有研究显示血清组氨酸水平降低可能与疾病活动度相关,但其机制和补充治疗的益处尚未明确。
- 肾功能衰竭:在慢性肾病患者中,组氨酸可能成为条件必需氨基酸,适当补充有助于改善贫血和营养状态。
总结:组氨酸是一个“多才多艺”的氨基酸。它不仅是构建蛋白质的普通砖石,其独特的化学性质使其成为生命催化剂(酶)中的关键“活性部件”;同时,它还是组胺等重要信号分子的直接前体,深刻影响着免疫、消化和神经系统功能。从分子催化到整体生理,组氨酸的作用无处不在。
ADFASDFAF23RQ23R
参考资料编辑本段
- Fersht, A. (1999). Structure and Mechanism in Protein Science: A Guide to Enzyme Catalysis and Protein Folding. W.H. Freeman.
- Krajewska, B. (2009). Mono-(Ag, Hg) and di-(Cu, Hg) valent metal ions effects on the activity of jack bean urease. Probing the modes of metal binding to the enzyme. Journal of Enzyme Inhibition and Medicinal Chemistry, 24(1), 1-10.
- Haas, H. L., Sergeeva, O. A., & Selbach, O. (2008). Histamine in the nervous system. Physiological Reviews, 88(3), 1183-1241.
- Thöny, B., & Blau, N. (2006). Mutations in the BH4-dependent aromatic amino acid hydroxylases. Annual Review of Genomics and Human Genetics, 7, 69-89.
- Wade, A. M., & Tucker, H. N. (1998). Antioxidant characteristics of L-histidine. The Journal of Nutritional Biochemistry, 9(6), 308-315.
- Mehler, A. H., & Tabor, H. (1953). Deamination of histidine to form urocanic acid in liver. Journal of Biological Chemistry, 201(2), 775-784.
- Visek, W. J. (1984). An update of concepts of essential amino acids. Annual Review of Nutrition, 4, 137-155.
- Zhu, B. T. (2002). On the general mechanism of selective inhibition of histidine decarboxylase by alpha-fluoromethylhistidine. Medical Hypotheses, 59(3), 305-311.
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。