细胞色素C
细胞色素C(Cytochrome c,简称Cyt c)是一种高度保守的线粒体蛋白,分子量约12.5 kDa,由核基因组编码、胞质核糖体合成前体后转运至线粒体。其成熟形式包含104个氨基酸残基(人类)及一个共价结合的血红素辅基,血红素铁原子以五配位方式与His18和Met80配位,呈现典型的三维结构:五个α-螺旋围绕血红素形成紧密的球形折叠,Cys14和Cys17通过硫醚键将血红素乙烯基侧链固定于蛋白骨架。这种结构赋予Cyt c两个关键功能:电子传递和凋亡信号转导。
分子结构与理化性质编辑本段
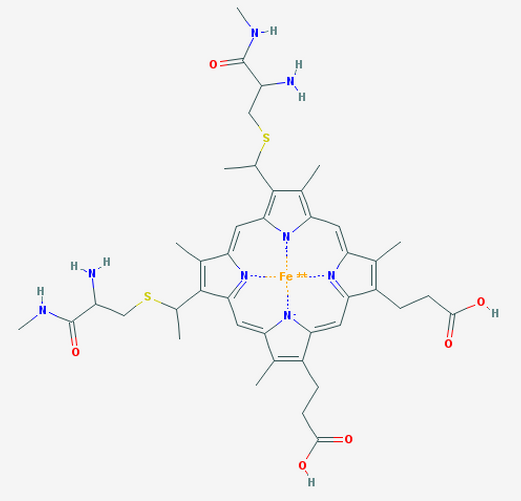
细胞色素C
Cyt c属于Ⅰ类细胞色素c家族,其血红素为c型血红素(铁-原卟啉Ⅸ),铁原子在氧化态(Fe³⁺)与还原态(Fe²⁺)之间切换,标准氧化还原电位约为+0.25 V(pH 7.0)。蛋白表面带有大量正电荷(pI≈10.0),利于与线粒体内膜上的负电荷磷脂(如心磷脂)相互作用。独特的Met80-铁配键在电子传递中交替断裂与重组,这一“开关”机制基于His18和Met80的轴向配位动态变化。X射线晶体学显示(PDB: 3ZCF),Cyt c具有高度保守的折叠模式,其整体结构在不同物种间相似度超过50%。
电子传递与能量代谢编辑本段
在氧化磷酸化过程中,Cyt c定位于线粒体内膜外表面,作为泛醌-细胞色素c还原酶(复合体Ⅲ)与细胞色素c氧化酶(复合体Ⅳ)之间可移动的电子穿梭体。复合体Ⅲ通过Q循环将电子从还原型泛醌(UQH₂)传递给Cyt c(每次传递一个电子),同时将质子泵入膜间隙。还原型Cyt c随后沿内膜扩散至复合体Ⅳ,在其CuA和血红素a₃中心处将电子传递至氧气,最终生成水。该过程伴随质子梯度的建立,驱动ATP合酶合成ATP。每分子Cyt c每次携带一个电子,其快速扩散系数(约10⁻⁷ cm²/s)及与复合体Ⅲ/Ⅳ的静电结合(Kd≈10⁻⁶ M)确保了高效的电子流通。缺少Cyt c的酵母突变体无法进行有氧呼吸,表明其在能量代谢中的必需性。
线粒体凋亡中的核心角色编辑本段
1996年,王晓东团队发现Cyt c释放是激活caspase的关键步骤。在凋亡诱导条件下(如DNA损伤、缺氧、生长因子撤除),Bax/Bak寡聚化导致线粒体外膜通透化(MOMP),Cyt c从膜间隙释放至胞质。胞质中的Cyt c与凋亡蛋白酶激活因子1(Apaf-1)、dATP/ATP结合,促使Apaf-1七聚化形成“凋亡体”(apoptosome)。凋亡体作为分子平台,通过CARD结构域招募并激活procaspase-9,活化的caspase-9进一步剪切下游效应caspase-3/7,执行细胞解体。此外,Cyt c的释放受Bcl-2家族蛋白精细调控:抗凋亡成员(Bcl-2、Bcl-xL)抑制MOMP,而促凋亡成员(Bid、Bim)促进释放。值得注意的是,Cyt c在胞质中还会与磷脂酰丝氨酸(PS)相互作用,增强其促凋亡活性。
翻译后修饰与功能调控编辑本段
Cyt c的活性受多种翻译后修饰(PTMs)调节:磷酸化(如Tyr97磷酸化降低电子传递效率)、亚硝化(Cys14/Cys17亚硝基化抑制凋亡释放)、乙酰化(Lys残基乙酰化影响与心磷脂结合)、氧化(Met80氧化导致血红素配位改变)。例如,在心肌缺血再灌注损伤中,活性氧(ROS)导致Cyt c的Met80氧化和血红素降解,加速凋亡进程。此外,Cyt c可被线粒体蛋白酶Lon(LONP1)降解,从而维持线粒体质量控制。
与非凋亡功能编辑本段
除能量代谢和凋亡外,Cyt c还参与:线粒体自噬——释放的Cyt c可与Parkin协同诱导线粒体自噬;抗氧化防御——还原型Cyt c可直接清除超氧阴离子;表观调控——胞质Cyt c可能影响组蛋白修饰酶的活性;免疫调控——释放的Cyt c作为损伤相关分子模式(DAMP)激活炎症小体。这些功能拓展了Cyt c在细胞稳态中的多维角色。
相关疾病与临床意义编辑本段
Cyt c功能异常与多种疾病相关:癌症——肿瘤细胞常通过上调抗凋亡蛋白或突变Cyt c逃逸凋亡(如Tyr97突变见于部分白血病);神经退行性疾病——阿尔茨海默病中Cyt c洩漏加剧神经元死亡;心肌缺血——再灌注时Cyt c大量释放导致心功能障碍;遗传病——COX4I2突变导致Cyt c氧化还原紊乱引发线粒体脑肌病。临床上,血清Cyt c水平作为凋亡标志物辅助诊断急性心肌梗死和脓毒症。此外,靶向Cyt c释放的小分子(如Bcl-2抑制剂Venetoclax)已用于白血病治疗。
研究技术编辑本段
Cyt c研究常用方法包括:光谱学(紫外-可见吸收光谱监测氧化还原状态);X射线晶体学/核磁共振解析结构;荧光标记(如EGFP-Cyt c融合蛋白追踪释放);免疫印迹/ELISA检测亚细胞定位;电化学(循环伏安法测定氧化还原电位);基因编辑(CRISPR-Cas9敲除或点突变分析功能)。
研究前沿与挑战编辑本段
当前热点包括:Cyt c与心磷脂相互作用的分子机制(是否驱动其构象变化);释放后的Cyt c如何避免被抗氧化系统清除;利用合成生物学改造Cyt c优化电子传递效率;开发新型Cyt c靶向药物(如稳定其还原态以抑制凋亡)。未来研究需整合多组学数据以阐明Cyt c网络的系统调控。
参考资料编辑本段
- Liu, X., Kim, C. N., Yang, J., Jemmerson, R., & Wang, X. (1996). Induction of apoptotic program in cell-free extracts: requirement for dATP and cytochrome c. Cell, 86(1), 147-157.
- Ow, Y. P., Green, D. R., Hao, Z., & Mak, T. W. (2008). Cytochrome c: functions beyond respiration. Nature Reviews Molecular Cell Biology, 9(7), 532-542.
- Kagan, V. E., Tyurin, V. A., Jiang, J., Tyurina, Y. Y., Ritov, V. B., Amoscato, A. A., ... & Borisenko, G. G. (2005). Cytochrome c acts as a cardiolipin oxygenase required for release of proapoptotic factors. Nature Chemical Biology, 1(4), 223-232.
- Gonzalvez, F., & Gottlieb, E. (2007). Cardiolipin: setting the beat of apoptosis. Apoptosis, 12(5), 877-885.
- Kuwana, T., & Newmeyer, D. D. (2003). Bcl-2-family proteins and the role of mitochondria in apoptosis. Current Opinion in Cell Biology, 15(6), 691-699.
- Mootha, V. K., Wei, M. C., Buttle, K. F., Scorrano, L., Panoutsakopoulou, V., Mannella, C. A., & Korsmeyer, S. J. (2001). A reversible component of mitochondrial respiratory dysfunction in apoptosis can be rescued by exogenous cytochrome c. The EMBO Journal, 20(4), 661-671.
- Jiang, X., & Wang, X. (2004). Cytochrome c-mediated apoptosis. Annual Review of Biochemistry, 73, 87-106.
- Salvesen, G. S., & Dixit, V. M. (1997). Caspases: intracellular signaling by proteolysis. Cell, 91(4), 443-446.
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
