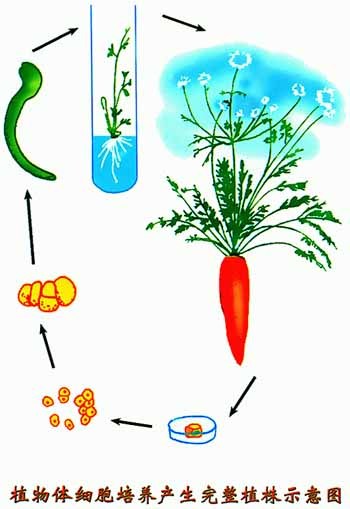
细胞全能性
定义与基本概念编辑本段
细胞全能性(cell totipotency)是生物体发育过程中最基础的细胞属性之一,指单个细胞具备在适宜条件下分裂、分化并最终发育成一个完整生物个体的潜能。与多能性(pluripotency)和单能性(unipotency)等术语不同,全能性强调细胞不仅能产生所有胚层(外、中、内胚层)和生殖细胞,还能形成胚外组织(如胎盘、滋养层),从而独立完成胚胎发生直至成体的全部过程。在动物体内,真正的全能性细胞仅存在于受精卵(合子)及少数早期卵裂球中,如小鼠2-细胞期卵裂球、人桑椹胚细胞。在植物界,这一现象更为普遍,许多成熟薄壁细胞甚至单倍体花粉细胞均可通过脱分化恢复全能性,进而形成完整植株。
历史与里程碑编辑本段
细胞全能性的概念可追溯至1902年德国胚胎学家汉斯·施派曼的蝶螈胚胎结扎实验,他通过分离早期卵裂球,证实单个细胞具备发育成完整个体的能力。1958年,英国科学家约翰·格登运用核移植技术,将非洲爪蟾蝌蚪肠上皮细胞核植入去核卵母细胞,成功培育出正常蝌蚪,首次证明已分化细胞的基因组仍保留全能遗传信息。1997年,伊恩·威尔穆特团队培育出体细胞核移植绵羊“多莉”,彻底颠覆了“分化不可逆”的传统教条。2006年,山中伸弥利用四种转录因子(Oct4、Sox2、Klf4、c-Myc)将小鼠成纤维细胞重编程为诱导多能干细胞(iPSCs),为规避伦理争议的全能性研究开辟新路径。中国科学家在此领域亦贡献卓著:2011年,周琪团队通过化学小分子组合(如VC、TGF-β抑制剂等)将小鼠成纤维细胞直接重编程为具有胚外组织形成能力的多能干细胞,接近全能态;2017年,邓宏魁团队开发化学重编程新体系(“3iL”方案),将人成纤维细胞转化为化学诱导多能干细胞(CiPSCs),其甲基化模式接近受精卵。
分子机制编辑本段
全能性的建立、维持与退出受多层级精密调控。在转录层面,核心网络由OCT4、SOX2、NANOG构成的正反馈环路主导,这些因子协同激活干性相关基因(如FOXD3、SALL4),同时抑制分化启动因子(如GATA6、SOX17)。表观修饰层面,全能性细胞的染色质呈现高度开放与可塑性:组蛋白H3K4me3广泛分布,H3K27me3抑制性标记富集程度低,DNA甲基化水平在早期卵裂期急剧下降并伴随全局去甲基化(如TET酶活性升高)。在2-细胞期特有的MERVL逆转录转座子被激活,其长末端重复序列(LTR)可作为增强子招募转录因子(如ZSCAN4、DUX4)促进全能性维持。此外,miRNA和LncRNA介导的后转录调控也参与其中,例如miR-291a-3p能协同Oct4、Sox2和Klf4提高iPSCs的诱导效率。信号通路方面,LIF/STAT3、TGF-β/Activin、Wnt/β-catenin通路在维持未分化状态中协同作用;而FGF/MAPK、PI3K/Akt通路的抑制或适度激活是启动全面分化程序的前提。
研究方法编辑本段
评估细胞全能性的金标准是嵌合体形成实验与四倍体补偿实验:将候选细胞(如iPSCs)注射入扩张囊胚,若该细胞能贡献于包括胚外组织在内的所有胚胎谱系,则表明其具备全能性。近年发展的单细胞RNA-seq和单细胞ATAC-seq技术可追踪早期胚胎中全能性细胞的转录组与染色质状态动态。化学重编程通过优化小分子组合(如GSK-3抑制剂CHIR99021、组蛋白去乙酰化酶抑制剂VPA等)逐步替代遗传因子,正成为非整合、低致瘤风险的技术方向。同时,三维索氏细胞培养(如集成微流控类胚胎系统)也在模拟早期发育环境以实现全能性维持方面取得进展。
应用与挑战编辑本段
细胞全能性在再生医学中价值巨大:全能性来源的器官构建、疾病特异性全能干细胞库、药物毒性体外筛选等均依赖对全能性机制的深入理解。但当前挑战不容忽视:iPSCs重编程效率普遍不足1%,且易出现表观记忆残留和基因组不稳定;体外获取的人类全功能全能干细胞仍无法支持胚外组织形成,其分化潜能不能完全体现。此外,全能性研究(特别是人胚胎干细胞的获取与核移植技术)在世界各地面临不同的法律与伦理制约,如美国NIH联邦基金不得用于创建或破坏人胚胎的科研项目。未来,通过阐明2-细胞期特异调控因子、优化化学递送系统以及开发非整合型重编程技术,有望突破现有瓶颈,实现安全高效的细胞全能性操控。
参考资料编辑本段
- Spemann H. Embryonic Development and Induction. New Haven: Yale University Press, 1938.
- Gurdon JB. The developmental capacity of nuclei taken from intestinal epithelium cells of feeding tadpoles. Journal of Embryology and Experimental Morphology, 1962, 10: 622-640.
- Wilmut I, Schnieke AE, McWhir J, et al. Viable offspring derived from fetal and adult mammalian cells. Nature, 1997, 385(6619): 810-813.
- Takahashi K, Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell, 2006, 126(4): 663-676.
- Shi Y, Inoue H, Wu JC, et al. Induced pluripotent stem cell technology: a decade of progress. Nature Reviews Drug Discovery, 2017, 16(2): 115-130.
- Hikabe O, Hamazaki N, Nagamatsu G, et al. Reconstitution in vitro of the entire cycle of the mouse female germ line. Nature, 2016, 539(7628): 299-303.
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。